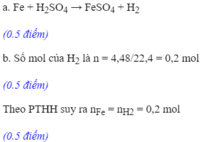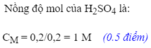1.Hòa tan a gam BaSO3 vào 500g dung dịch axit HCl dư. Sau phản ứng thu được 4,48 lít khí SO2 ở đktc.
a. Tính a=?
b. Tính nồng độ % của axit tham gia phản ứng.
c. Tính nồng độ % của dung dịch muối tạo thành sau phản ứng.
2. Hòa tan hoàn toàn 21,6 gam hốn hợp gồm Mg và MgO cần dùng 400ml dung dịch HCl. Sau phản ứng thấy có 8,96 lít khí H2 thoát ra ở (đktc).
a. Viết PT pư xảy ra.
b. Tính khối lượng mỗi chất có trong hỗn hợp.
c. Tính % khối lượng mỗi chất có trong hỗn hợp.
d. Tính nồng độ mol của dung dịch HCl tham gia pư.
đ. Coi thể tích dung dịch không đổi tính nồng độ mol của dung dịch muối thu được sau pư?
3. Hòa tan 19,2g hốn hợp bột kim loại Mg và Fe cần 400g dung dịch HCl 7,3%.
a. Viết PTHH xảy ra.
b. Tính thể tích khí H2 thoát ra ở đktc?
c. Tính % theo khối lượng từng chất có trong hỗn hợp?